专题 | 脊髓性肌萎缩症(SMA)与基因检测
![]() 浏览次数:0
浏览次数:0
![]() 日期:2017.03.24
日期:2017.03.24
技术资讯
专题 | 脊髓性肌萎缩症(SMA)与基因检测
![]() 浏览次数:0
浏览次数:0
![]() 日期:2017.03.24
日期:2017.03.24
脊髓性肌萎缩症(Spinal Muscular Atrophy, SMA)是一种常染色体隐性遗传的神经肌肉病, 临床特征是脊髓前角细胞变性退化、导致对称性肌无力和肌萎缩,为一种常见的运动神经元疾病,主要表现为肌肉萎缩、肌张力低、腱反射减弱、病理征阴性,目前尚无有效治疗手段。
SMA通常根据疾病严重程度与发病年龄分为三个亚型。 I型患者(MIM#253300)在出生时或在6个月之前开始发病,不能独自坐或走,并且通常在两年内死于呼吸功能不全。II型患者(MIM# 253550)在6个月之后发病,可以独坐但在没有任何辅助设备帮助的情况下不能走路,并且寿命会大大减少,III型患者(MIM# 253400)通常在1岁半后发病,可以独立的坐或走路,但在青春期或成人后一般行走能力有所退步,需要靠轮椅行动。
脊髓性肌萎缩症在人群中的携带率约为1/35-1/50左右,发病率约为1/6000-1/10000左右。
SMA与基因
目前遗传学已经确认,SMA主要与两个高度同源(是指这两个基因的序列非常相似)的基因密切相关,SMN1与SMN2,这两个基因主要通过7号外显子和8号外显子上的两个基因位点进行区分(下图来自Qu YJ et al, PMID: 27425821, J Mol Diagn,2016)。
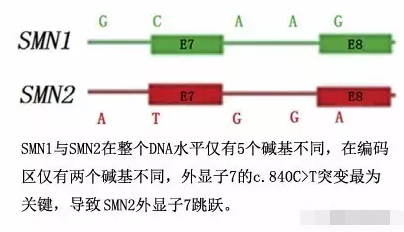
一般来说,大部分正常个体都有2份拷贝的SMN1基因与2份拷贝的SMN2基因, SMN2基因发生外显子7的跳跃,只有少量的全长SMN mRNA,所以如果某个人两份拷贝的SMN1基因都失去功能的话一定会患病,只有一份SMN1基因起作用的个体为携带者。在SMN1基因都失去功能的情况下,SMN2基因拷贝数数目,则会影响患者的发病时间与疾病严重程度。根据Feldkötter et al. (Am J of Hum Genetics, 2002)描述,80%的I型SMA患者携带有1到2个SMN2拷贝,82%的II型SMA患者携带有3个SMN2拷贝,96%的III型SMA患者携带有3或4个SMN2拷贝。所以对于SMA患者来说,检测SMN2基因的拷贝数在一定程度上有助于评估疾病的严重性或预后。等等,你们已经发现以上内容有问题了,怎么会有4个SMN2拷贝呢?为了便于大家理解,上面提到大部分正常人的2份SMN2拷贝,由于基因所在区域的复杂性,实际上人群中SMN2拷贝数在0到4个。根据统计95%以上的SMA患者都会检测到SMN1基因外显子7和(或)外显子8纯合缺失,除此之外,还有复合杂合突变(一个等位基因缺失,另一个点突变)。
当你理解了以上内容后,还有一些比较复杂的情况,首先SMN1基因外显子7的那个独特碱基(c. 840C)可以由C转换为T,这样SMN1基因就变成了SMN2基因,从造成的结果上来说,这个转换与缺失的效果是一样的,但是对于患者来说就多了一个SMN2拷贝,其次,人群中有很低比例的正常人一条染色体上有2个SMN1拷贝,而另外一条染色体上为0个拷贝,这样的正常人SMN1基因型为2+0,其实也是携带者,但是目前没有切实可行的方法去区分1+1还是2+0,但是有一个位点与之高度关联,也许将来三代测序可以。当你了解了以上内容后,我们再来聊聊SMA基因检测,理想的基因检测应该达到如下效果:
1 明确区分患者、携带者、正常人;
2 如果为SMN1纯合缺失患者,能够检测SMN2拷贝数;
3 除了检测SMN1外显子7缺失或转换外,还能检测点突变;
4 可以识别SMN12+0基因型的特殊携带者;
SMA基因检测的方法有以下几类
PCR-RFLP或一代测序
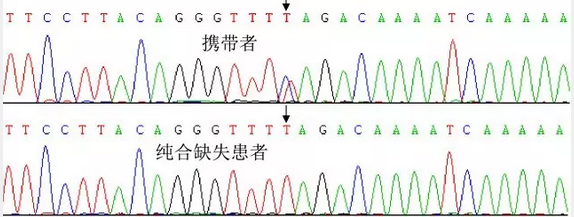
首先对目标区域进行扩增,然后通过限制性内切酶或一代测序的方法来区分,如果是患者的样本,在c.840位点缺失SMN1的C峰,只显示SMN2的T纯合峰,正常人或携带者应该为杂合的C/T峰图,RFLP的分析方法性价比并不高,是那时唯一可以采用的新方法,替代SSCP分析。这个方法有个缺陷,就是有酶切不彻底的隐患,但是不能区分携带者与正常人,也不能检测SMN2拷贝数,在临床上可以诊断SMN1纯合缺失的患者,其他情况只能作为初筛。
 双侧双重AS-PCR
双侧双重AS-PCR
该方法是由黄尚志老师带领团队开发,利用 SMN1与 SMN2基因中外显子7与内含子7的 2 处核苷酸差别, 分别设计 2个等位基因特异的引物,与内对照直接 在琼脂糖电泳及 PAGE进行分析, 获得很好的效果。 由于设计的引物正反向均有与 SMN1 基因特异碱基结合的位点 ,应用两个引物对模板的选择性, 增强了特异性。与酶切方法比较, 诊断结果完全一致, 但没有非特异扩增,避免了酶切不完全的缺点 ,且方法简便, 易操作,适宜临床使用。

荧光定量PCR
主要原理是通过两个多重实时荧光定量PCR反应,以单拷贝RPP40基因为内标基因,采用MGB-Taqman探针法分别对SMN1基因第7和第8外显子进行拷贝数相对定量,来判断是否发生缺失或转换。
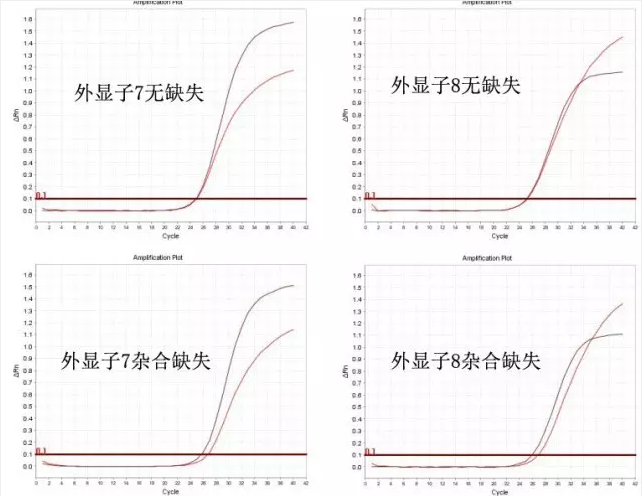
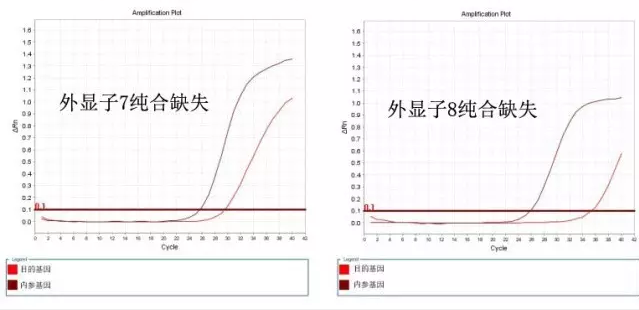
(图来自上海五色石医学研究股份有限公司官网)
优势是可以区分患者,携带者、正常人,其他如SMN1点突变和2+0基因型携带者也不能检测。患者的SMN2拷贝数需要另外设计探针进行检测。
MLPA
多重连接探针扩增技术(multiplex ligation-dependent probe amplification ,MLPA)于2002年由Schouten等首先报道,是早年几年发展起来的一种针对待检DNA序列进行定性和半定量分析的新技术。该技术高效、特异,在一次反应中可以检测45个核苷酸序列拷贝数的改变,针对c.840C>T位点设计不同的探针序列,SMN1基因扩增子和SMN2基因扩增子可以扩增出不同的片段长度,而峰的高度可以反映拷贝数变异。
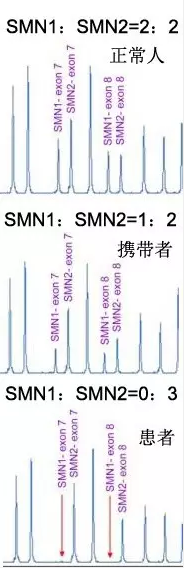
(图片来自Genetics in Med 2007:9(4)241-248)
MLPA技术除明确区分患者、携带者及正常人,同时检测患者的SMN2拷贝数,。目前临床上MLPA是SMA基因检测金标准,但是该试剂盒不能检测点突变与特殊的SMN1 2+0携带者。
PCR-DHPLC
DHPLC是一种基因突变筛查技术,既能够自动化、高通量进行,且除PCR之外,勿需进行PCR引物修饰、购买特殊试剂、检测标记信号或作其它的样品处理。DHPLC具有高通量检测、自动化程度高、灵敏度和特异性较高、检测DNA片段和长度变动范围广、相对价廉等优点。苏一宁等(pmid:15832310)通过针对c.840C>T位点设计特异性引物扩增SMN基因片段,结合峰高与内参基因来确定SMN1与SMN2拷贝数。
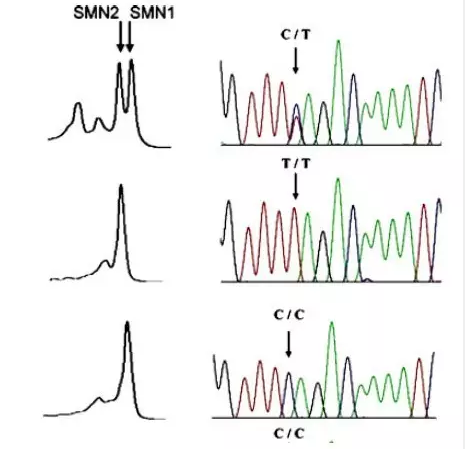
(图片来自苏一宁等,pmid:15832310)
PCR-DHPLC与MLPA类似可以明确区分患者、携带者及正常人,也可以检测患者的SMN2拷贝数。
二代测序
最近贝勒医学院的研究者在Genetics in Medicine杂志上发表了一项利用二代测序检测SMA的研究(pmid:28125085),该研究包括6648例样本。主要的原理是统计SMN1与SMN2总拷贝数,然后根据c.840C>T分析SMN1 reads与SMN2 reads比例,最后得出每个人分别携带几个拷贝的SMN1与SMN2。与MLPA相比,灵敏度大于98%,特异性大于98%。另外该研究还确诊了几个致病点突变位点,并且g.27134T>G与RFLP结果一致,该位点与SMN1 2+0型特殊携带者密切相关。但是对于SMN2拷贝数的灵敏度与特异性未明确描述,可能是因为该研究的目的主要是筛查,而非临床诊断。
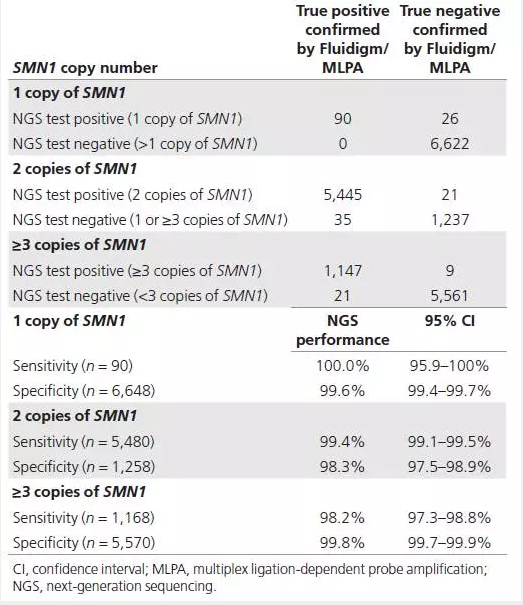
(图片来自Feng Y et al,Genet Med. 2017)
临床上,很多肌肉疾病和SMA的表型容易混淆,难以鉴别,传统的MLPA等检测方法仅能定向检测SMA,而全外显子测序这类NGS技术不仅可以定向检出SMA,还可以同时覆盖其他相关表型的类似肌病,这是一个优势,当然NGS技术目前尚不能说是完美, NGS可以作为初筛诊断SMA和其他肌病的有效方法,但初筛疑似阳性的结果还需要进行MLPA或Sanger测序的验证。另外在SMN2拷贝数分析方面,NGS还有待更多的证据证明其准确性和可靠性。
最后
本文整理了SMA相关资料与各基因检测平台的比较,随着测序成本的下降,通过全外显子或大Panel进行遗传病筛查与诊断已经成为趋势,而对于大片段缺失重复的疾病如果能够通过算法优化检测将让NGS性价比更高,在临床上,对于SMA患者,还需要MLPA验证及确定SMN2拷贝数。
本文来自网络转载
上一篇:自然流产的遗传学检查和咨询
下一篇:染色体多态